Translationale Hautkrebsforschung
Prof. Dr. Dr. Jürgen Becker
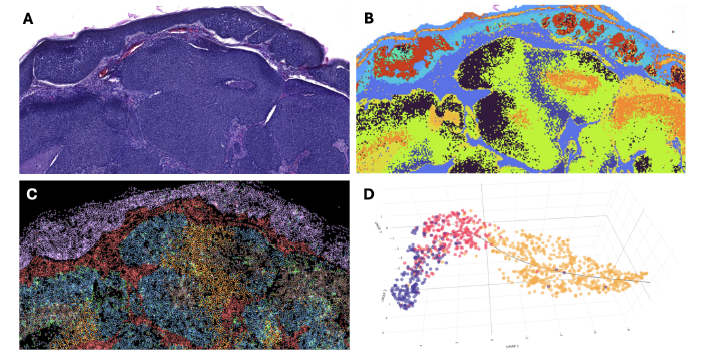
Hautkrebs bietet besondere Möglichkeiten für die translationale Krebsforschung. Die meisten Tumoren werden früh erkannt, die Krankheitsverläufe sind stufenweise (lokoregionale Metastasen gehen Fernmetastasen voraus), und selbst in fortgeschrittenen Stadien bestehen Hautläsionen häufig parallel zu viszeralen Metastasen. Diese Charakteristika erlauben eine detaillierte Untersuchung von Tumorgeweben mit modernsten Methoden. Dabei lassen sich nicht nur die Tumorzellen selbst, sondern auch deren Mikroumgebung (Tumor-Mikromilieu, TME), insbesondere das Immunsystem, präzise analysieren.
Krebs ist nicht lediglich eine Ansammlung von Tumorzellen, sondern das Ergebnis komplexer Wechselwirkungen zwischen Stromazellen, Immunzellen und neoplastischen Zellen. Diese Interaktionen bestimmen sowohl den Krankheitsverlauf als auch die Wirksamkeit von Therapien.
Früher konnten solche Zusammenhänge nur mithilfe von Modellsystemen untersucht werden, z. B. patientenabgeleiteten Mausmodellen, CAM-Modellen, Tumororganoiden oder Tumor-on-a-Chip-Technologien. Obwohl diese Modelle wichtige Einblicke ermöglichen, bleiben sie künstlich und spiegeln die Situation im Patienten nur bedingt wider.
Mit den jüngsten technischen Fortschritten – wie Einzelzell-Multiomics (scRNA-seq, scATAC-seq, scM&T-seq, REAP-seq), räumlicher Transkriptomik und Phänotomik – sowie integrativen Analysemethoden (z. B. Joint Latent Variable- oder Bayes-Modelle) ist es nun möglich, ex vivo umfassende funktionelle Analysen von patientenbasiertem Tumorgewebe durchzuführen. Besonders wertvoll sind hierbei Proben aus gezielten, niedrig-interventionellen klinischen Studien (LIT, nach EU-Verordnung Nr. 536/2014; z. B. FieldCancerization oder CemiFirst) sowie aus begleitenden translationalen Forschungsprogrammen zu klinischen Studien (z. B. IMMUNED oder ADMEC). Auch archiviertes FFPE-Gewebe aus prospektiv angelegten Geweberegistern (z. B. MCC TRIM) kann inzwischen detailliert analysiert werden.
Diese Ansätze haben zur Identifizierung neuer Biomarker beigetragen – darunter Surrogatmarker (Tumorlast, Früherkennung), prognostische Marker (klinischer Spontanverlauf) und prädiktive Marker (Therapieansprechen). Darüber hinaus konnten neue therapeutische Strategien entwickelt werden, etwa die kombinierte Hemmung von DNA-Reparatur und DNA-Schadensantwort oder die Induktion einer neuroblastischen Transformation von MCC-Zellen.
Unsere Ergebnisse deuten außerdem darauf hin, dass der Einsatz von Immuntherapien in sehr frühen Krankheitsstadien – sogar noch vor einer adjuvanten Behandlung – das klinische Outcome erheblich verbessern könnte. Dieser Ansatz wird demnächst in einer klinischen Studie geprüft, die von einem umfassenden translationalen Forschungsprogramm begleitet wird.
Zukünftige Projekte und Ziele
In den letzten Jahren ist es gelungen, eine prospektive Sammlung klinisch annotierter Bioproben von Hauttumoren aufzubauen, die zum Teil sequenziell und unter definierten Bedingungen entnommen wurden. Dadurch lassen sich dynamische Veränderungen im Tumor und seiner Mikroumgebung abbilden. Diese Proben werden nun genutzt, um zentrale Fragen zu beantworten, wie nach der räumlichen Verteilung von Tumorheterogenität, dem Einfluss endogener Retroviren auf die Wirksamkeit von Immuntherapien oder der Rolle des lokalen Mikrobioms für das Tumorwachstum.
Solche Studien sind sehr aufwendig, kostenintensiv und datenintensiv. Daher ist geplant, Teile der Untersuchungen auf Gewebemikroarrays (TMAs) durchzuführen. Mittels Mikro-CT wird dabei zunächst ein 3D-Überblick über die Gewebestruktur erstellt, um eine optimale Positionierung der Gewebekerne zu gewährleisten. Gleichzeitig erlaubt dieser Ansatz, die Ergebnisse der Multi-Omics-Analysen wieder in den dreidimensionalen Gewebekontext zurückzuprojizieren.

Prof. Dr. Dr. Jürgen C. Becker
Abteilungsleiter – Partnerstandort Essen/Düsseldorf
Universität Duisburg – Essen Biologische Fakultät
Translationale Hautkrebsforschung / Translational Oncology (Skin Cancer Research)