Krebsgenomforschung
Prof. Dr. Holger Sültmann
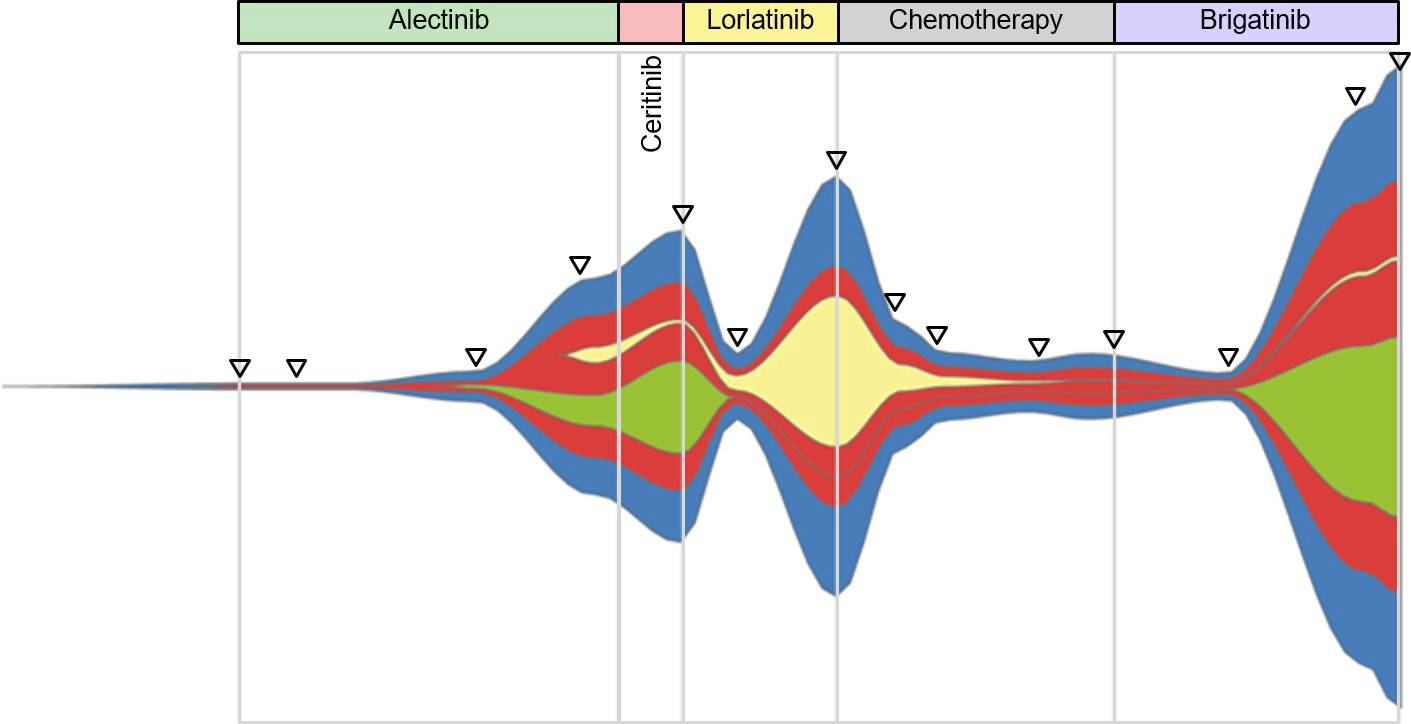
Die Entwicklung von Tumoren geht mit molekularen Veränderungen auf genomischer, epigenomischer und Genexpressions-Ebene einher. Ziel unserer Forschung ist es, diese molekularen Veränderungen zu identifizieren, ihre Rolle bei der Entstehung und dem Fortschreiten von Tumoren zu verstehen und sie in Diagnostik, Prognose und Vorhersage von Krebserkrankungen zu übersetzen.
Unsere Forschung umfasst die genomweite Analyse molekularer Veränderungen in verschiedenen Krebsentitäten mit Schwerpunkt auf Lungen- und Brusttumoren. Wir wenden Hochdurchsatz-Technologien für DNA- und RNA-Sequenzierungen in Gewebe- und Blutproben („Liquid Biopsy“) an, um die räumliche und zeitliche Tumorheterogenität zu charakterisieren. Die identifizierten epigenomischen, genomischen und transkriptomischen Marker werden für eine individuelle Risikostratifizierung und personalisierte klinische Betreuung der Patient:innen genutzt.
Um die Rolle dieser molekularen Veränderungen im Tumorprogress und der Therapie-Resistenz zu verstehen, verwenden wir zelluläre 3D-Kokulturmodelle sowie eine Vielzahl zell- und molekularbiologischer Methoden.
Unsere Arbeit wird durch starke Kooperationen mit Partnern aus dem klinischen Bereich (z. B. Onkologie, Chirurgie, Radiologie, Radioonkologie) und der Wissenschaft (z. B. „-Omics“, Einzelzell- und räumliche Biologie, computergestützte Biologie, KI) unterstützt.
Zukünftige Projekte und Ziele
In der personalisierten und präventiven Onkologie ist die Erkennung minimaler Residualerkrankungen von großer Bedeutung, um die Therapie entsprechend anpassen zu können. Wir sind überzeugt, dass diese Herausforderung nur durch die Integration individueller Patientendaten wie etwa Lebensstil, radiologische Bildgebung und molekulare Marker gelöst werden kann, idealerweise unterstützt durch KI-Algorithmen.
Daher ist das Ziel unserer zukünftigen Forschung, longitudinale Serum- und Plasmaproben zu nutzen, um neuartige Multi-Marker-Panels zu identifizieren, die (epi)genomische, fragmentomische, proteomische und metabolomische Merkmale umfassen, und so die Risikostratifizierung von Krebspatient:innen zu verbessern. Um die Translation in die klinische Anwendung zu erleichtern, werden wir unsere Kooperationen mit klinischen und wissenschaftlichen Partnern weiter ausbauen, insbesondere am Nationalen Centrum für Tumorerkrankungen (NCT), um eine solide Grundlage für die Anwendung von Liquid Biopsy in klinischen Studien zu schaffen.
