Experimentelle und Translationale Tumorimmunologie
Prof. Dr. Gerald Willimsky
Die Entwicklung klinisch relevanter Mausmodelle sowie die Analyse der spontanen und therapieinduzierten Immunantwort gegen nicht transplantierte Tumore sind zentrale Ziele dieser Arbeitsgruppe.
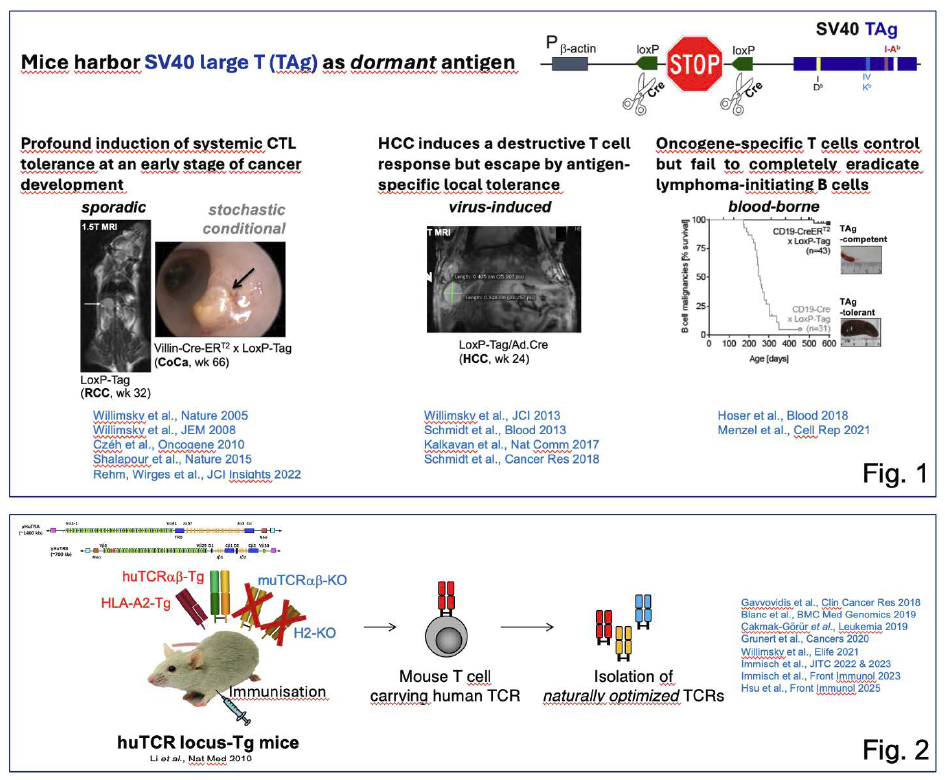
Krebszellen können von T-Zellen erkannt werden, was durch den Erfolg von Checkpoint-Inhibitoren wie Anti-CTLA-4 (anti-cytotoxisches T-Lymphozyten-Antigen 4) und Anti-PD-1 (anti-programmed death 1) eindrucksvoll bestätigt wurde. Ob destruktive oder nicht-destruktive spontane T-Zell-Antworten im autochthonen Wirt ausgelöst werden, hängt von den Entzündungsbedingungen ab, unter denen die Tumore entstehen. So zeigte die primäre Krebsentwicklung mit konditionaler Krebsantigenexpression mittels Cre/LoxP-System in genetisch veränderten Mausmodellen einerseits eine ausgeprägte tumorausgelöste systemische Toleranz bereits im prämalignen Stadium sporadischer Tumore. Andererseits konnte die Induktion systemischer Immunität, aber lokale, antigenspezifische zytotoxische T-Zell-Toleranz (CTL) bei virusinduzierten Tumoren beobachtet werden. Beim Zusammenwirken von CD4-T-Zellen in Klasse-I- und Klasse-II-doppelpositiven Lymphomen fanden wir eine Art Immunüberwachung (Abb. 1).
Für die klinische Translation liegt unser Fokus auf der TCR-Gentherapie, entweder durch adoptive T-Zell-Therapie oder bispezifische Antikörperformate. Dies beinhaltet die Identifikation immunogener Zielantigene sowie neue Methoden der therapeutischen Genübertragung (CRISPR/Cas- und mRNA-Technologien) zur Bekämpfung von Krebs und viralen Erkrankungen. Mithilfe einer einzigartigen humanen TCR-transgenen Mausplattform (Abb. 2) haben wir T-Zell-Rezeptor-Bibliotheken mit natürlich optimierter Affinität gegenüber tumor-spezifischen und tumor-assoziierten Antigenen generiert. Geeignete TCRs sollen für die klinische Anwendung weiterverfolgt werden.
Zukünftige Projekte und Ziele
Zukünftig sollen spontane und therapieinduzierte T-Zell-Antworten in autochthonen Krebsmodellen sowohl in Gegenwart als auch Abwesenheit chronischer Entzündungen untersucht werden. Dies erfolgt unter Einfluss verschiedener Ernährungsweisen (metabolische Effekte) sowie in Anwesenheit eines natürlichen Mikrobioms (Wildling-Mausmodell).
Mit der Erweiterung der TCR-Generierungsplattform auf Mäuse, die verschiedene MHC Klasse I- und Klasse II-Moleküle tragen, erwarten wir künftig eine „praxisverändernde“ kombinierte CD8+/CD4+ Krebsimmuntherapie.
Die Etablierung der CRISPR/Cas-vermittelten, nicht-viralen Genmodifikation von T-Zellen in geschlossenen Produktionssystemen wird die komplexen GMP-Strukturen auf ein Minimum reduzieren und somit eine kostengünstigere und schnellere klinische Anwendung von T-Zell-Therapien ermöglichen.

Prof. Dr. Gerald Willimsky
Charité – Universitätsmedizin Berlin / DKFZ
Experimentelle und Translationale Tumorimmunologie / Experimental and Translational Tumor Immunology