RadPlanBio: Eine integrierte Plattform für translationale Krebsforschung
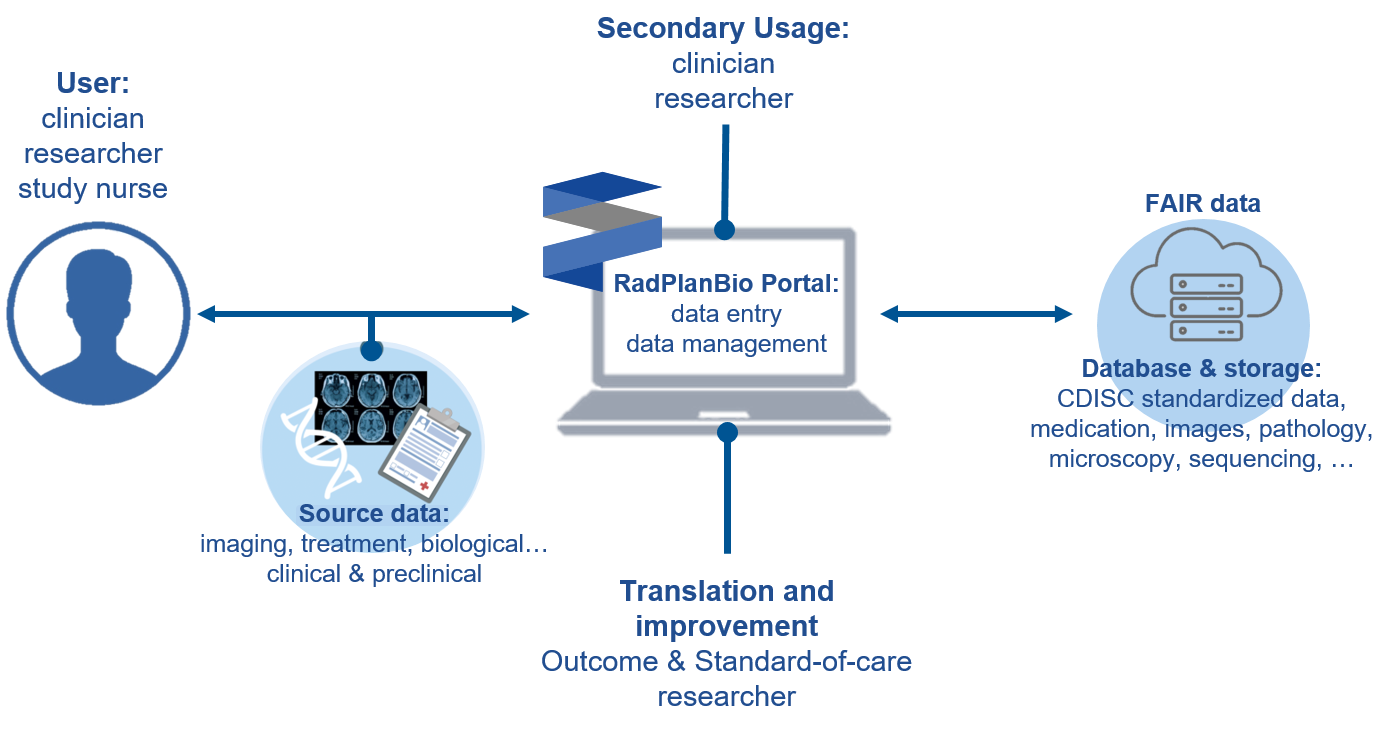
Die DKTK Plattform RadPlanBio bietet eine umfassende, webbasierte Umgebung für das Datenmanagement zur Unterstützung präklinischer und klinischer Krebsstudien innerhalb des DKTK und darüber hinaus. RadPlanBio deckt ein breites Spektrum translationaler Forschungsanforderungen ab, indem unterschiedliche Datentypen integriert werden – darunter medizinische Bildgebung, Bestrahlungs- und Behandlungspläne, Laboranalysen, genomische Daten sowie klinische Endpunkte. Damit eignet sich die Plattform sowohl für klinische Studien als auch für präklinische Forschung einschließlich Tiermodellen.
Durch die Zusammenführung dieser Daten ermöglicht RadPlanBio, Laborbefunde systematisch mit Patientendaten zu verknüpfen und Krankheitsmechanismen besser zu verstehen.
Ein Beispiel ist die interventionelle DELPHI-Studie, in der eine reduzierte adjuvante Therapie bei HPV-positivem Oropharynx-Plattenepithelkarzinom untersucht wird. RadPlanBio gewährleistet hier eine strukturierte Datendokumentation sowie eine verlässliche Zuordnung zu Behandlungsgruppen. Die Plattform unterstützt Dummy-Runs und die Qualitätssicherung von Therapieplänen und stellt so die Protokolltreue über mehrere Zentren hinweg sicher. Darüber hinaus ermöglicht sie ein strukturiertes Datenmonitoring und integriert Biomarkererhebungen mit klinischen und strahlentherapeutischen Daten. Dies schafft eine belastbare Grundlage für translationale Analysen.
Auch für präklinische Studien unterstützt RadPlanBio sowohl retrospektive als auch prospektive Dokumentation, einschließlich transparenter Behandlungsgruppenzuweisung. In der präklinischen NIMO-Studie, die prognostische Biomarker für das Ansprechen auf Nimorazol in Kombination mit Radiochemotherapie in HNSCC-Xenograft-Modellen untersucht, ermöglicht RadPlanBio die Bestimmung von Tumorkontrollraten und integriert Biomarkerdaten wie Transkriptomik, Methylomik und histologische Parameter (z. B. hypoxisches Volumen, Gefäßdichte, Perfusion). Durch die Kombination dieser Datensätze schafft RadPlanBio eine robuste Grundlage zur Identifikation prädiktiver Biomarker und zur Überführung präklinischer Erkenntnisse in die klinische Forschung.
Die Plattform wird kontinuierlich weiterentwickelt, um semantische Technologien zu integrieren und sich an etablierten Standards auszurichten, darunter Good Clinical Practice (GCP) und die CDISC-Richtlinien zur Datenstandardisierung. Ein elektronisches Case Report Form (eCRF)-System stellt eine konsistente Datenerhebung sowie die Einhaltung klinischer Standards und datenschutzrechtlicher Vorgaben sicher. Ein zentrales Data Warehouse speichert die erhobenen Daten in standardisierter Struktur und gewährleistet die Umsetzung der FAIR-Prinzipien. So können Forschende ihre Daten effizient explorieren und analysieren.
RadPlanBio wird synchron am DKTK-Standort Dresden und am DKFZ in Heidelberg sicher betrieben. Die Plattform unterstützt standortübergreifende Zusammenarbeit durch kontrollierten Datenaustausch in mono- und multizentrischen klinischen sowie präklinischen Studien und Projekten.
Wenn Sie Biomarker untersuchen, therapeutische Kombinationen evaluieren oder umfassende Outcome-Analysen durchführen möchten, bietet RadPlanBio eine verlässliche und etablierte Infrastruktur für Ihr Forschungsvorhaben. Das RadPlanBio-Team lädt Forschende ein, ihre Projekte in dieser kooperativen Umgebung weiterzuentwickeln.
Kontakt
Für alle Anfragen, eine Beratung oder weitere Informationen kontaktieren Sie bitte: radplanbio@dkfz-heidelberg.de
Koordination Dresden

Prof. Dr. Mechthild Krause
Abteilungsleiterin – Partnerstandort Dresden

Dr. Antje Dietrich
Wissenschaftliche Koordinatorin Dresden
OncoRay – Nationales Zentrum für Strahlenforschung in der Onkologie
Koordination Heidelberg
Registrierte Software:
https://helmholtz.software/software/radplanbio
Weitere Links:
https://www.dkfz.de/radioonkologie-radiobiologie/radplanbio
https://www.oncoray.de/de/netzwerk/deutsches-konsortium-fuer-translationale-krebsforschung-dktk/hnpraedbio-studie-und-radplanbio-plattform
Ausgewählte Publikationen:
Plattform
Skripcak T, Belka C, Bosch W, Brink C, Brunner T, Budach V, Büttner D, Debus J, Dekker A, Grau C, Gulliford S, Hurkmans C, Just U, Krause M, Lambin P, Langendijk JA, Lewensohn R, Lühr A, Maingon P, Masucci M, Niyazi M, Poortmans P, Simon M, Schmidberger H, Spezi E, Stuschke M, Valentini V, Verheij M, Whitfield G, Zackrisson B, Zips D, Baumann M. Creating a data exchange strategy for radiotherapy research: towards federated databases and anonymised public datasets. Radiother Oncol. 2014 Dec;113(3):303-9. doi: 10.1016/j.radonc.2014.10.001.
Skripcak T, Just U, Schönfeld I, Troost EGC, Krause M. Storage and databases for big data, chpt. 3, Big Data in Radiation Oncology, 1st Edition CRC press, 2019, https://doi.org/10.1201/9781315207582
Giraldo O, Sabyrrakhim A, Roscher M, Euler-Lange R, Baumann M, Kurth I, Hadiwikarta WW.
Semantic Representation of Preclinical Data in Radiation Oncology. ICBO 2024, Enschede, The Netherlands, July 18-19 2024, CEUR-WS.org, online https://CEUR-WS.org/Vol-3939/short2.pdf
Klinisch
Löck S, Linge A, Lohaus F, Ebert N, Gudziol V, Nowak A, Tinhofer I, Kalinauskaite G, Guberina M, Stuschke M, Balermpas P, von der Grün J, Grosu AL, Debus J, Ganswindt U, Belka C, Peeken JC, Combs SE, De-Colle C, Zips D, Baretton GB, Krause M, Baumann M; Biomarker signatures for primary radiochemotherapy of locally advanced HNSCC - Hypothesis generation on a multicentre cohort of the DKTK-ROG. Radiother Oncol. 2022 Apr;169:8-14. doi: 10.1016/j.radonc.2022.02.009.
Tawk B, Rein K, Schwager C, Knoll M, Wirkner U, Hörner-Rieber J, Liermann J, Kurth I, Balermpas P, Rödel C, Linge A, Löck S, Lohaus F, Tinhofer I, Krause M, Stuschke M, Grosu AL, Zips D, Combs SE, Belka C, Stenzinger A, Herold-Mende C, Baumann M, Schirmacher P, Debus J, Abdollahi A. DNA-Methylome-Based Tumor Hypoxia Classifier Identifies HPV-Negative Head and Neck Cancer Patients at Risk for Locoregional Recurrence after Primary Radiochemotherapy. Clin Cancer Res. 2023 Aug 15;29(16):3051-3064. doi: 10.1158/1078-0432.CCR-22-3790.
Martin D, Schreckenbach T, Ziegler P, Filmann N, Kalinauskaite G, Tinhofer I, Budach V, Gani C, Zips D, Schimek-Jasch T, Schäfer H, Grosu AL, Thomas E, Krause M, Dapper H, Combs S, Hoffmann C, Stuschke M, Walter F, Belka C, Kurth I, Hadiwikarta WW, Baumann M, Rödel C, Fokas E. Evaluation of prognostic factors after primary chemoradiotherapy of anal cancer: A multicenter study of the German Cancer Consortium-Radiation Oncology Group (DKTK-ROG).
Radiother Oncol. 2022 Feb;167:233-238. doi: 10.1016/j.radonc.2021.12.050.
Präklinisch
José Besso M, Bitto V, Koi L, Wijaya Hadiwikarta W, Conde-Lopez C, Euler-Lange R, Bonrouhi M, Schneider K, Linge A, Krause M, Baumann M, Kurth I. Transcriptomic and epigenetic landscape of nimorazole-enhanced radiochemotherapy in head and neck cancer. Radiother Oncol. 2024 May 30:110348. doi: 10.1016/j.radonc.2024.110348.
Bitto V, Hönscheid P, Besso MJ, Sperling C, Kurth I, Baumann M, Brors B. Enhancing mass spectrometry imaging accessibility using convolutional autoencoders for deriving hypoxia-associated peptides from tumors. NPJ Syst Biol Appl. 2024 May 27;10(1):57. doi: 10.1038/s41540-024-00385-x.
Koi L, Bitto V, Weise C, Möbius L, Linge A, Löck S, Yaromina A, Besso MJ, Valentini C, Pfeifer M, Overgaard J, Zips D, Kurth I, Krause M, Baumann M. Prognostic biomarkers for the response to the radiosensitizer nimorazole combined with RCTx: a pre-clinical trial in HNSCC xenografts. J Transl Med. 2023 Aug 26;21(1):576. doi: 10.1186/s12967-023-04439-2. PMID: 37633930
